El proceso de Haber-Bosch consiste en la síntesis de amoniaco a partir de nitrógeno e hidrógeno, en condiciones de elevada presión (200 atm) y elevada temperatura (450-500ºC). La reacción que tiene lugar es:
N2(g) + 3H2(g) ↔ 2 NH3(g) -92,2 KJ
 Para que la reacción tenga lugar se utilizan diversos catalizadores, principalmente compuestos de hierro, aunque también óxidos de aluminio y de potasio. El nitrógeno que se usa como reactivo se obtiene directamente del aire. El hidrógeno se obtiene a partir de un hidrocarburo, siendo el gas natural la materia prima más utilizada para este fin. En el caso del metano, componente principal del gas natural, la reacción que tiene lugar es:
Para que la reacción tenga lugar se utilizan diversos catalizadores, principalmente compuestos de hierro, aunque también óxidos de aluminio y de potasio. El nitrógeno que se usa como reactivo se obtiene directamente del aire. El hidrógeno se obtiene a partir de un hidrocarburo, siendo el gas natural la materia prima más utilizada para este fin. En el caso del metano, componente principal del gas natural, la reacción que tiene lugar es:
CH4(g) + H2O(g) ↔ CO(g) + 3H2(g)
El monóxido de carbono generado debe ser eliminado. Este paso es muy importante, ya que si no se lleva a cabo podría acortar considerablemente la vida útil del catalizador. Bosch solventó este problema convirtiendo previamente el CO en CO2, y realizando posteriormente un sistema de lavados con lejías cupríferas que permiten la absorción de ambos compuestos. La conversión de CO en CO2 se produce mediante la siguiente reacción:
CO(g) + H2O(g) ↔ CO2(g) + H2(g)
El proceso de Haber-Bosch lleva utilizándose más de 100 años, y sin embargo sigue sin comprenderse por completo cómo tiene lugar la reacción de síntesis de amoniaco en la superficie de los catalizadores. El pasado mes de noviembre la revista Science publicó un artículo en el que un grupo de científicos de la Universidad de Rochester y del Instituto Max Planck de Química Bioinorgánica aportan nueva luz sobre los eventos que tienen lugar, a escala molecular, durante la síntesis de este compuesto a partir de sus elementos. “El proceso de Haber-Bosch es eficiente, pero es difícil de comprender, porque la reacción ocurre sólo en la superficie del catalizador, y esto es difícil de estudiar directamente”, afirma Patrick Holland, investigador principal del estudio.
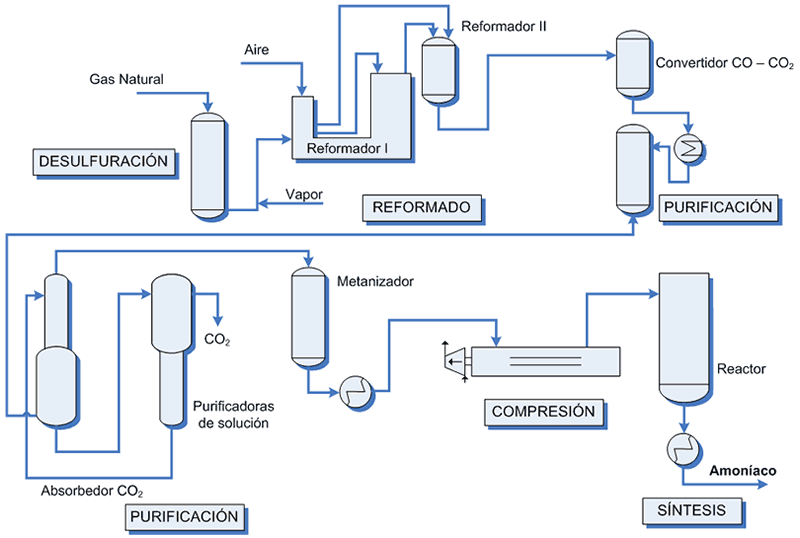
Video acerca de una Planta de Amoniaco:
https://www.youtube.com/watch?v=TixVXNDaUlU
Bibliografia.-
Ing. Palacios (2007). Recuperado de http://triplenlace.com/2011/12/12/como-se-produce-amoniaco-proceso-haber-bosch/#sthash.Gt1gCrXv.dpuf



